本品為人血液制品,因原料來(lái)自人血,雖然對(duì)原料血漿進(jìn)行了相關(guān)病原體的篩查,并在生產(chǎn)工藝中加入了去除和滅活病毒的措施,但理論上仍存在傳播某些已知和未知病原體的潛在風(fēng)險(xiǎn),臨床使用時(shí)應(yīng)權(quán)衡利弊。
>國(guó)內(nèi)首家血液制品GMP認(rèn)證企業(yè)
>國(guó)內(nèi)首家采用雙重病毒滅活工藝用于生產(chǎn)
>國(guó)內(nèi)首家采用全自動(dòng)采漿機(jī)和全自動(dòng)洗瓶滅菌罐裝生產(chǎn)線的生產(chǎn)企業(yè)
>血漿優(yōu)質(zhì)安全,多道ELISA(酶聯(lián)免疫法)和核酸擴(kuò)增技術(shù)檢測(cè)
>不含防腐劑和抗生素,純度高,穩(wěn)定性好
>全面與世界接軌的標(biāo)準(zhǔn)化體系認(rèn)證

請(qǐng)仔細(xì)閱讀說(shuō)明書并在醫(yī)師指導(dǎo)下使用
本品為人血液制品,因原料來(lái)自人血,雖然對(duì)原料血漿進(jìn)行了相關(guān)病原體的篩查,并在生產(chǎn)工藝中加入了去除和滅活病毒的措施,但理論上仍存在傳播某些已知和未知病原體的潛在風(fēng)險(xiǎn),臨床使用時(shí)應(yīng)權(quán)衡利弊。
[藥品名稱]
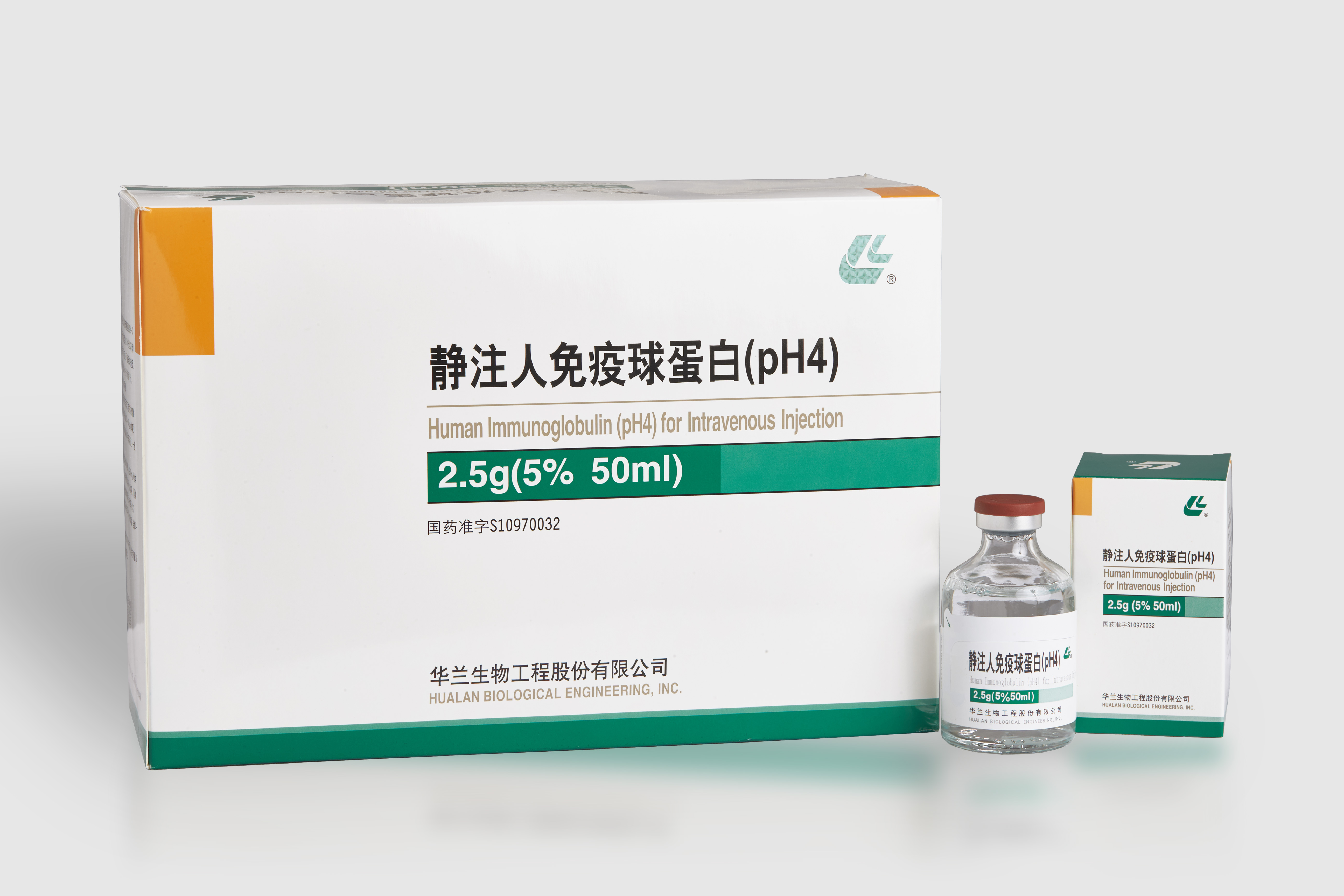
通用名稱:靜注人免疫球蛋白(pH4)
英文名稱:Human Immunoglobulin (pH4) for Intravenous Injection
漢語(yǔ)拼音:Jingzhu Ren Mianyiqiudanbai(pH4)
[成份]
本品活性成份為人免疫球蛋白,主要是IgG,輔料為聚山梨酯80、麥芽糖、注射用水。
[性狀]
本品應(yīng)為無(wú)色或淡黃色澄明液體,可帶輕微乳光,不應(yīng)出現(xiàn)渾濁。
[適應(yīng)癥]
1.原發(fā)性免疫球蛋白缺乏癥,如X聯(lián)鎖低免疫球蛋白血癥,常見變異性免疫缺陷病,免疫球蛋白G亞型缺陷病等。
2.繼發(fā)性免疫球蛋白缺陷病,如重癥感染,新生兒敗血癥等。
3.自身免疫性疾病,如原發(fā)免疫性血小板減少癥,川崎病。
[規(guī)格]
2.5g/瓶(5%,50ml)
[用法用量]
用法:靜脈滴注或以5%葡萄糖溶液稀釋1~2倍作靜脈滴注,開始滴注速度為1.0ml/分鐘(約20滴/分鐘)持續(xù)15分鐘后若無(wú)不良反應(yīng),可逐漸加快速度,最快滴注速度不得超過(guò)3.0ml/分鐘(約60滴/1分鐘)。
用量:遵醫(yī)囑。
推薦劑量:
1.原發(fā)性免疫球蛋白缺乏或低下癥:首次劑量:400mg/kg體重;維持劑量:200~400mg/kg體重,給藥間隔時(shí)間視病人血清IgG水平和病情而定,一般每月一次。
2.原發(fā)免疫性血小板減少癥:每日400mg/kg體重,連續(xù)5日。維持劑量每次400mg/kg體重,間隔時(shí)間視血小板計(jì)數(shù)和病情面定,一般每周一次。
3.重癥感染:每日200~300mg/kg體重,連續(xù)2~3日。
4.川崎病:發(fā)病10日內(nèi)應(yīng)用,兒童治療劑量2.0g/kg體重,一次輸注。
[不良反應(yīng)]
輸注時(shí)可能出現(xiàn)一過(guò)性頭痛、心慌、惡心等不良反應(yīng),可能與輸注速度過(guò)快或個(gè)體差異有關(guān)。上述反應(yīng)大多發(fā)生在輸注開始一小時(shí)內(nèi),因此建議在輸注的全過(guò)程定期觀察患者的一般情況和生命體征,必要時(shí)應(yīng)減慢或暫停輸注,一般無(wú)需特殊處理即可自行恢復(fù)。 個(gè)別患者可在輸注結(jié)束后發(fā)生上述反應(yīng),一般在24小時(shí)內(nèi)均可自行恢復(fù)。
1.國(guó)外臨床試驗(yàn)
同類的國(guó)外上市產(chǎn)品在超過(guò)5%的臨床試驗(yàn)受試者中觀察到以下常見不良反應(yīng):頭痛、寒戰(zhàn)、發(fā)熱、疼痛、乏力、背痛、思心、嘔吐、腹痛、腹瀉、輸液部位反應(yīng)、皮疹、瘙癢、蕁麻疹、高血壓、低血壓、心動(dòng)過(guò)速等。
2.國(guó)內(nèi)上市后監(jiān)測(cè)
本品及同類的國(guó)內(nèi)上市產(chǎn)品監(jiān)測(cè)到如下不良反應(yīng)事件,由于這些不良反應(yīng)/事件是在無(wú)法確定總數(shù)的人群中自發(fā)報(bào)告的,因此不能準(zhǔn)確估算其發(fā)生率:
(1)全身性損害:畏寒,高熱、胸痛、不適、蒼白、乏力、眶周水腫、水腫、全身酸痛等。
(2)皮膚及其附件損害:斑丘疹、紅斑性皮疹、局限性皮膚反應(yīng)、表皮松解、多發(fā)性紅斑、皮炎(如大皰性皮炎)、出汗增加等。
(8)免疫功能紊亂和感染:過(guò)敏反應(yīng)、過(guò)敏樣反應(yīng)、輸液反應(yīng)、過(guò)敏性休克等。
(4)心血管系統(tǒng)損害:紫紺、心悸、高血壓、心律失常等。
(5)神經(jīng)系統(tǒng)損害:頭暈、昏迷、意識(shí)喪失、震顫、肌肉不自主收縮、感覺減退等。
(6)呼吸系統(tǒng)損害:呼吸困難、呼吸急促、呼吸暫停、喘息、喉頭水腫、呼吸功能不全、輸血相關(guān)急性肺損傷、低氧血癥等。
(7)血管損害和出凝血障礙:潮紅、靜脈炎等。
(8)精神障礙:激越、精神障礙、嗜睡等。
(9)代謝和營(yíng)養(yǎng)障礙:高血糖。(注:藥品成份中含糖類的,注明此項(xiàng))
( 10)血液系統(tǒng)損害:白細(xì)胞減少、中性粒細(xì)胞減少、粒細(xì)胞缺乏等。
3.國(guó)外上市后監(jiān)測(cè)
同類的國(guó)外上市產(chǎn)品還監(jiān)測(cè)到如下不良反應(yīng)事件,由于這些不良反應(yīng)事件是在無(wú)法確定總數(shù)的人群中自發(fā)報(bào)告的,因此不能準(zhǔn)確估算其發(fā)生率:
(1)皮膚及其附件損害:史蒂文斯-約翰遜綜合征等。
(2)神經(jīng)系統(tǒng)損害:癲癇發(fā)作、無(wú)菌性腦膜炎等。
(3)呼吸系統(tǒng)損害:急性呼吸窘迫綜合征、肺水腫、支氣管痙攣等。
(4)血管損害和出凝血障礙:血栓形成等。
(5)血液系統(tǒng)損害:血漿黏度增加、溶血反應(yīng)等。
(6)泌尿系統(tǒng)損害:腎功能損害等。
[禁忌]
1.對(duì)人免疫球蛋白過(guò)敏或有其他嚴(yán)重過(guò)敏史者。
2.有抗IgA抗體的選擇性IgA缺乏者。
[注意事項(xiàng)]
1.本品專供靜脈輸注用。
2.如需要,可以用5%葡萄糖溶液稀釋本品,但糖尿病患者應(yīng)慎用。
3.藥液呈現(xiàn)混濁、沉淀、異物或瓶子有裂紋、過(guò)期失效等情況下,不得使用。
4.本品開啟后,應(yīng)一次輸注完畢,不得分次或給第二人輸用。
5.有嚴(yán)重酸堿代謝紊亂的患者應(yīng)慎用。
6.監(jiān)測(cè)急性腎功能衰竭患者的腎功能,包括血尿素氮、血肌酐和尿量。對(duì)于腎功能不全或衰竭的患者,要以最小的速度輸注。易感患者使用本品可能引起腎功能異常。
7.可能發(fā)生血栓性事件。監(jiān)測(cè)有血栓形成事件已知危險(xiǎn)因素的患者;對(duì)有高粘血癥風(fēng)險(xiǎn)患者的血液粘度進(jìn)行基線評(píng)估。對(duì)于有血栓形成風(fēng)險(xiǎn)的患者,要在最小劑量下緩慢輸注。
8.可能發(fā)生無(wú)菌性腦膜炎綜合征,特別是在高劑量或快速輸注時(shí)。
9.可能發(fā)生溶血性貧血。監(jiān)測(cè)溶血和溶血性貧血患者的臨床體征和癥狀。
[孕婦及哺乳期婦女用藥]
未專門進(jìn)行該項(xiàng)針對(duì)性試驗(yàn)研究,且無(wú)系統(tǒng)可靠的參考文獻(xiàn)。對(duì)孕婦或可能懷孕婦女的用藥應(yīng)慎重,如有必要應(yīng)用時(shí),應(yīng)在醫(yī)師指導(dǎo)和嚴(yán)密觀察下使用。
[兒童用藥]
未專門進(jìn)行該項(xiàng)針對(duì)性試驗(yàn)研究,且無(wú)系統(tǒng)可靠的參考文獻(xiàn)。
[老年用藥]
未進(jìn)行該項(xiàng)試驗(yàn)研究,且無(wú)系統(tǒng)可靠的參考文獻(xiàn)。在65歲以上的患者中,一般情況下,不超過(guò)推薦劑量,緩慢輸注。
[藥物相互作用]
本品尚無(wú)與其它藥物相互作用的臨床研究資料。因此本品須嚴(yán)格單獨(dú)輸注,不得與其他任何藥物混合使用。
為了避免被動(dòng)接受本品中特異性抗體的干擾,輸注本品3個(gè)月后才能接種某些減毒活疫苗,如脊髓灰質(zhì)炎、麻疹、風(fēng)疹、腮腺炎以及水痘病毒疫苗等。基于同樣的考慮,在非緊急狀態(tài)下,已經(jīng)接種了這類疫苗的患者至少在接種后3~4周才能輸注本品;如果在接種后3~4周內(nèi)使用了本品,則應(yīng)在最后一次輸注本品后3個(gè)月重新接種。
[藥物過(guò)量]
未專門進(jìn)行該項(xiàng)針對(duì)性試驗(yàn)研究,且無(wú)系統(tǒng)可靠的參考文獻(xiàn)。過(guò)量使用可能導(dǎo)致患者循環(huán)血容量超載和血液粘度增高而增加心臟的負(fù)荷,此結(jié)果更常見于老年患者和腎功能損傷患者。
[藥理毒理]
本品含有廣譜病毒、細(xì)菌或其他病原體的IgG抗體,經(jīng)靜脈輸注后,能迅速提高受者血液中的IgG水平,增強(qiáng)機(jī)體的抗感染能力和發(fā)揮免疫調(diào)節(jié)功能。
[藥代動(dòng)力學(xué)]
未專門進(jìn)行該項(xiàng)針對(duì)性試驗(yàn)研究。文獻(xiàn)報(bào)道,人免疫球蛋白生物半衰期約為3~4周。
[貯藏]
于2~8°C避光保存和運(yùn)輸。
[包裝]
硼硅玻璃模制注射劑瓶、澳化丁基橡膠塞包裝。1瓶/盒。
[有效期]
自生產(chǎn)之日起36個(gè)月。
[執(zhí)行標(biāo)準(zhǔn)]
YBS10392020
[批準(zhǔn)文號(hào)]
國(guó)藥準(zhǔn)字S10970032
[上市許可持有人]
名稱:華蘭生物工程股份有限公司
注冊(cè)地址:河南省新鄉(xiāng)市華蘭大道甲1號(hào)
[生產(chǎn)企業(yè)]
企業(yè)名稱:華蘭生物工程股份有限公司
生產(chǎn)地址:河南省新鄉(xiāng)市華蘭大道甲1號(hào)
郵政編碼:4530030
電話號(hào)碼:(0373) 3519992
傳真號(hào)碼:(0373) 3519991
網(wǎng)址: http://m.xingchedou.cn